Struktur dan Perkembangan Model Atom: Dalton, Thomson, Rutherford, Bohr, dan Modern
Pijar Belajar
||0 Minute Read|Review
0
Dalam pembelajaran kimia, salah satu metode pembelajaran yang harus kalian pahami dan ketahui adalah struktur dan model atom. Atom sendiri adalah unsur kimia terkecil yang dapat berdiri sendiri dan dapat bersenyawa dengan yang lain. Nah, mengetahui struktur dan model atom ini sangat penting, lho, dalam bidang kimia.
Yuk, simak penjelasan di bawah ini untuk mengetahui struktur dan model atom!
Baca juga: Materi Kimia Kelas 10 - Reaksi Redoks: Oksidasi dan Reduksi
Mengenal Struktur Atom dan Model Atom
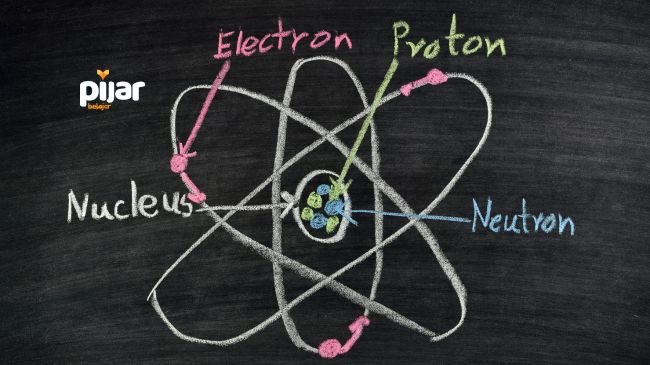
Mungkin diantara kalian banyak yang belum paham dan tahu apa sih struktur atom itu. Jadi, pada dasarnya struktur atom merupakan susunan partikel dasar dalam atom. Istilah atom sendiri berarti sebagai benda keberadaan partikel terkecil dari suatu materi yang tidak bisa dibagi lagi. Nah, struktur atom sendiri terdiri dari tiga partikel yang lebih kecil, yakni proton, neutron, dan elektron.
Nah dalam struktur atom ini, ada beberapa model atom yang perlu kamu pahami dan ketahui secara mendalam. Yuk, kenalan dengan model-model atom berikut ini. .
Model Atom Dalton
Model atom yang paling sederhana adalah model atom dalton. Model atom dalton ini dikemukakan oleh seorang ilmuwan asal Inggris, yaitu John Dalton. Model atom dalton ini memiliki bentuk bola pejal yang tidak bermuatan. Selain itu, menurut teori ini, atom merupakan kesatuan terkecil yang tidak bisa dibagi-bagi lagi, sehingga unsur kimia yang berbeda akan memiliki jenis atom yang berbeda-beda pula.
Sayangnya, teori Dalton sulit digunakan untuk menjelaskan cara atom sebagai bola pejal dapat menghantarkan arus listrik. Padahal, listrik adalah elektron yang bergerak. Dalton sendiri tak sempat membuktikan partikel lain yang menghantarkan arus listrik. Oleh karena itu, teori model atom dalton ini dipatahkan oleh ilmuwan setelahnya.
Model Atom Thomson
Model atom Thomson ditemukan oleh Joseph John Thomson. Model atom Thomson berbentuk seperti roti kismis karena atom merupakan bola padat bermuatan positif dengan partikel negatif (elektron) yang tersebar di dalamnya. Lalu, model atom ini juga mengatakan bahwa muatan positif dan negatif pada atom memiliki jumlah sama. Model atom ini dibuktikan dengan penelitian Thomson yang menggunakan sinar tabung katoda.
Akan tetapi, model atom Thomson tidak dapat menjelaskan susunan muatan positif dan negatif dalam atom dalam penentuannya.
Model Atom Rutherford
Metode atom ini dikemukakan oleh oleh Ernest Rutherford pada tahun 1911. Dalam teori atom ini, setiap atom mengandung inti atom yang bermuatan positif dengan elektron yang mengelilingi dalam lintasannya. Lalu, massa atom ini terpusat di inti atom dan sebagian besar volume atom tersebut merupakan ruang hampa, lho. Hal ini dibuktikan dari hasil percobaan penembakan logam oleh sinar alpha, yang dikenal juga dengan Percobaan Geiger-Marsden.
Model atom Rutherford ini sejatinya tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan teori fisika, gerakan elektron mengitari inti ini disertai pemancaran energi. Ini menyebabkan lama-kelamaan energi elektron akan berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke dalam inti. Meski demikian, Rutherford telah berjasa mengenalkan konsep lintasan atau kedudukan elektron yang kelak disebut dengan kulit atom.
Model Atom Bohr
Model atom yang satu ini dicetuskan oleh Niels Bohr dan Ernest Rutherford pada tahun 1913. Dalam pengembangan model atom Bohr, dikatakan bahwa atom terdiri dari inti atom yang mengandung proton dan neutron dan dikelilingi oleh elektron yang berputar dalam orbitnya (tingkat energi tertentu). Orbit ini dikenal sebagai kulit atom.
Model atom Bohr ini memiliki radius dan orbit. Ini tidak sesuai dengan Prinsip Ketidakpastian Heisenberg yang menyatakan radius tidak bisa ada bersamaan dengan orbit. Selain itu, model atom Bohr juga tidak menjelaskan Efek Zeeman. Efek Zeeman adalah ketika garis spektrum terbagi karena adanya medan magnet.
Model Atom Modern
Model atom yang terakhir adalah Teori atom modern yang menganggap atom sebagai partikel dasar atau unit terkecil dari materi yang masih mempertahankan sifat kimia suatu unsur. Atom terdiri dari inti yang bermuatan positif yang terdiri dari proton dan neutron, serta elektron yang bermuatan negatif yang mengorbit di sekitar inti atom itu sendiri.
____________________________________________
Baca juga: Titrasi Asam Basa: Pengertian, Alat dan Bahan, Prosedur dan Contoh Soalnya
Nah setelah mengetahui struktur atom beserta berbagai model-model lainnya, tentunya sudah mulai kalian pahami dan ketahui pastinya. Mau penjelasan yang lebih lengkap lagi mengenai pembelajaran kimia lainnya seperti struktur atom ini? tentunya kalian bisa mengunduh aplikasi Pijar Belajar. Karena disini kalian bakal mendapat berbagi edukasi belajar dan contoh soal yang bisa kalian pelajari dan ketahui secara mendalam.
Tunggu apalagi, langsung saja download aplikasi Pijar Belajar sekarang. Dan aplikasi ini sangat cocok untuk belajar berbagai mata pelajaran khususnya untuk kelas 10 SMA.




